Europio, il simbolo è Eu e il numero atomico è 63. Come tipico membro dei lantanidi, l'europio ha solitamente valenza +3, ma è comune anche la valenza +2 dell'ossigeno. Esistono meno composti dell'europio con uno stato di valenza +2. Rispetto ad altri metalli pesanti, l'europio non ha effetti biologici significativi ed è relativamente atossico. La maggior parte delle applicazioni dell'europio sfrutta l'effetto fosforescente dei composti dell'europio. L'europio è uno degli elementi meno abbondanti nell'universo; ce ne sono solo circa 5 × 10-8% della sostanza.
L'europio esiste nella monazite
La scoperta dell'europio
La storia inizia alla fine del XIX secolo: a quel tempo, scienziati di eccellenza iniziarono a riempire sistematicamente i vuoti rimasti nella tavola periodica di Mendeleev analizzando lo spettro di emissione atomica. Oggi, questo compito non è difficile e può essere portato a termine da uno studente universitario; tuttavia, a quel tempo, gli scienziati disponevano solo di strumenti di bassa precisione e campioni difficili da purificare. Pertanto, per tutta la storia della scoperta dei lantanidi, tutti i "quasi" scopritori continuarono a fare affermazioni false e a discutere tra loro.
Nel 1885, Sir William Crookes scoprì il primo, seppur non chiarissimo, segnale dell'elemento 63: osservò una specifica riga spettrale rossa (609 nm) in un campione di samario. Tra il 1892 e il 1893, lo scopritore di gallio, samario e disprosio, Paul Émile LeCoq de Boisbaudran, confermò questa banda e scoprì un'altra banda verde (535 nm).
Successivamente, nel 1896, Eugène Anatole Demarçay separò pazientemente l'ossido di samario e confermò la scoperta di un nuovo elemento delle terre rare, situato tra il samario e il gadolinio. Separò con successo questo elemento nel 1901, segnando la fine del percorso di scoperta: "Spero di chiamare questo nuovo elemento Europio, con il simbolo Eu e una massa atomica di circa 151".
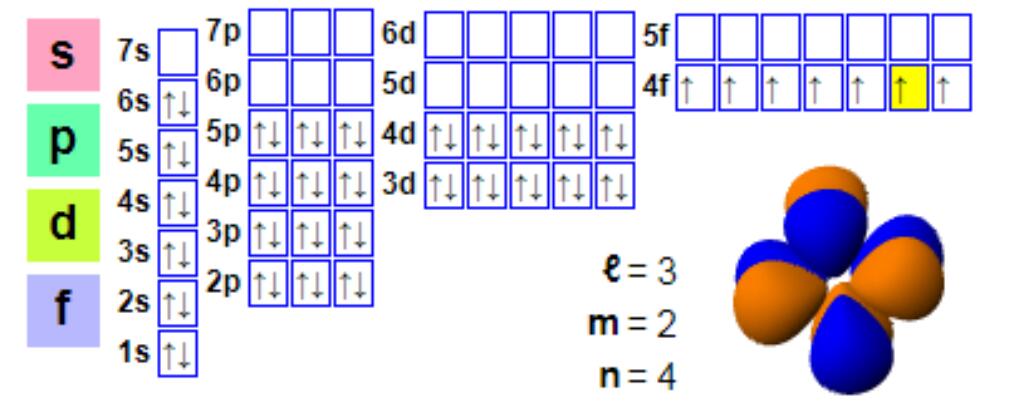
Configurazione elettronica
Configurazione elettronica:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f7
Sebbene l'europio sia solitamente trivalente, tende a formare composti bivalenti. Questo fenomeno è diverso dalla formazione di composti di valenza +3 da parte della maggior parte dei lantanidi. L'europio bivalente ha una configurazione elettronica 4f7, poiché il guscio f semiriempito fornisce maggiore stabilità, e l'europio (II) e il bario (II) sono simili. L'europio bivalente è un agente riducente debole che si ossida all'aria per formare un composto di europio (III). In condizioni anaerobiche, in particolare in condizioni di riscaldamento, l'europio bivalente è sufficientemente stabile e tende a essere incorporato nel calcio e in altri minerali alcalino-terrosi. Questo processo di scambio ionico è alla base della "anomalia negativa dell'europio", ovvero, rispetto all'abbondanza di condrite, molti minerali lantanidi come la monazite presentano un basso contenuto di europio. Rispetto alla monazite, la bastnaesite presenta spesso meno anomalie negative dell'europio, quindi la bastnaesite è anche la principale fonte di europio.
L'europio è un metallo grigio ferroso con un punto di fusione di 822 °C, un punto di ebollizione di 1597 °C e una densità di 5,2434 g/cm³; è l'elemento meno denso, più tenero e più volatile tra gli elementi delle terre rare. L'europio è il metallo più attivo tra gli elementi delle terre rare: a temperatura ambiente, perde immediatamente la sua lucentezza metallica nell'aria e si ossida rapidamente in polvere; reagisce violentemente con acqua fredda per generare idrogeno gassoso; l'europio può reagire con boro, carbonio, zolfo, fosforo, idrogeno, azoto, ecc.
Applicazione dell'europio
Il solfato di europio emette fluorescenza rossa sotto la luce ultravioletta
Georges Urbain, un giovane e brillante chimico, ereditò lo strumento di spettroscopia di Demarçay e scoprì che un campione di ossido di ittrio (III) drogato con europio emetteva una luce rossa molto intensa nel 1906. Questo è l'inizio del lungo viaggio dei materiali fosforescenti all'europio, utilizzati non solo per emettere luce rossa, ma anche luce blu, poiché lo spettro di emissione di Eu2+ rientra in questo intervallo.
Un fosforo composto da emettitori rossi Eu3+, verdi Tb3+ e blu Eu2+, o da una loro combinazione, può convertire la luce ultravioletta in luce visibile. Questi materiali svolgono un ruolo importante in vari strumenti in tutto il mondo: schermi di intensificazione dei raggi X, tubi a raggi catodici o schermi al plasma, così come le recenti lampade fluorescenti a risparmio energetico e i diodi a emissione luminosa.
L'effetto di fluorescenza dell'europio trivalente può essere sensibilizzato anche da molecole aromatiche organiche e tali complessi possono essere applicati in varie situazioni che richiedono elevata sensibilità, come inchiostri anticontraffazione e codici a barre.
Dagli anni '80, l'europio ha svolto un ruolo di primo piano nelle analisi biofarmaceutiche ad alta sensibilità utilizzando il metodo della fluorescenza fredda a tempo risolto. Nella maggior parte degli ospedali e dei laboratori medici, tali analisi sono diventate di routine. Nella ricerca nel campo delle scienze della vita, incluso l'imaging biologico, le sonde biologiche fluorescenti a base di europio e altri lantanidi sono onnipresenti. Fortunatamente, un chilogrammo di europio è sufficiente per supportare circa un miliardo di analisi: dopo che il governo cinese ha recentemente limitato le esportazioni di terre rare, i paesi industrializzati, presi dal panico per la carenza di terre rare nelle scorte, non devono più preoccuparsi di simili minacce per tali applicazioni.
L'ossido di europio viene utilizzato come fosforo a emissione stimolata in un nuovo sistema di diagnosi medica a raggi X. L'ossido di europio può anche essere utilizzato per produrre lenti colorate e filtri optoelettronici, per dispositivi di accumulo a bolle magnetiche e nei materiali di controllo, schermanti e strutturali dei reattori atomici. Poiché i suoi atomi possono assorbire più neutroni di qualsiasi altro elemento, è comunemente usato come materiale per l'assorbimento di neutroni nei reattori atomici.
Nel mondo odierno in rapida espansione, la recente scoperta dell'applicazione dell'europio potrebbe avere un profondo impatto sull'agricoltura. Gli scienziati hanno scoperto che le plastiche drogate con europio bivalente e rame monovalente possono convertire efficacemente la componente ultravioletta della luce solare in luce visibile. Questo processo è piuttosto verde (è il colore complementare del rosso). L'utilizzo di questo tipo di plastica per costruire una serra può consentire alle piante di assorbire più luce visibile e aumentare la resa delle colture di circa il 10%.
L'europio può essere applicato anche ai chip di memoria quantistica, in grado di memorizzare informazioni in modo affidabile per diversi giorni. Questi possono consentire di archiviare dati quantistici sensibili in un dispositivo simile a un disco rigido e di spedirli in tutto il paese.
Data di pubblicazione: 27 giugno 2023